Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124
Physical Address
304 North Cardinal St.
Dorchester Center, MA 02124
Le diagnostic immunologique, ou sérologie , repose sur un principe biologique fondamental : l’interaction spécifique de type clé-serrure du complexe antigène-anticorps (Ag-Ac) . Cette interaction est considérée comme un phénomène thermodynamique, avec des constantes d’affinité qui déterminent la sensibilité et la spécificité de chaque test, allant des simples tests de grossesse aux analyses auto-immunes complexes.
En clinique, on cherche rarement directement les « germes ». On s’intéresse plutôt à la réponse du système immunitaire à ces derniers. Cette réponse repose sur la liaison d’un épitope (sur l’antigène) à un paratope (sur l’anticorps).
Un échec diagnostique spécifique à l’immunologie, appelé « effet Prozone », est fréquemment rencontré en laboratoire.
Principe : Pour que des réactions visibles (précipitation ou agglutination) aient lieu, une structure réticulaire est nécessaire , dans laquelle les anticorps lient différents antigènes.⁴ Une telle structure se forme uniquement dans la zone d’équivalence (rapport optimal antigène/anticorps).
Shutterstock
Implication diagnostique : En cas de forte suspicion de la maladie malgré des résultats négatifs, le laboratoire doit diluer le sérum . Cette dilution réduit la concentration d’anticorps, permettant ainsi à l’échantillon de sortir de la Prozone et à la réaction de se produire.
Le tournant de l’immunologie a été le test ELISA (dosage immuno-enzymatique) , qui a révolutionné le domaine en convertissant la liaison biologique en un changement de couleur visible. Concrètement, il consiste à fixer une enzyme à l’anticorps.
Le test ELISA repose sur une phase solide (un puits en plastique) pour retenir la cible et sur un anticorps conjugué à une enzyme (généralement la peroxydase de raifort ou la phosphatase alcaline ) pour révéler sa présence.⁵ Lorsqu’un substrat est ajouté, l’enzyme le transforme en un produit coloré. L’intensité de la coloration ( densité optique ) est proportionnelle à la concentration de la cible.⁶
Shutterstock
diagnostic rapide (TDR), ou « tests à flux latéral », ont rendu les tests immunologiques accessibles à tous en les faisant sortir des laboratoires de haute technologie et en les amenant au chevet du patient. 13
Un RDT n’est pas simplement d’immunologie un morceau de papier ; c’est un dispositif microfluidique .
| Fonctionnalité | Norme de laboratoire (ELISA) | Test rapide (TDR) |
| Risque d’effet crochet | Rare (Les étapes de lavage éliminent l’excédent) | Risque courant : Une charge antigénique élevée peut saturer la bandelette, empêchant la liaison au niveau de la ligne de test ( faux négatif ). |
| Quantification | Précis (quantitatif) | Oui/Non (Qualitatif) |
L’un des domaines les plus complexes de l’immunologie diagnostique est l’auto-immunité , où le système immunitaire perd sa « tolérance au soi » et attaque l’hôte.
Le diagnostic des maladies auto-immunes est rarement établi par un seul test. 16 Il nécessite une approche par étapes.
Il s’agit du filet de pêche. Il détecte les anticorps ciblant le noyau de la cellule.
| Modèle | Trouble associé |
| Homogène | Lupus érythémateux systémique (LES) |
| Tacheté | Syndrome de Sjögren ou maladie mixte du tissu conjonctif |
| Nucléolaire | sclérodermie |
Certains anticorps ciblent spécifiquement certains tissus plutôt que le noyau.
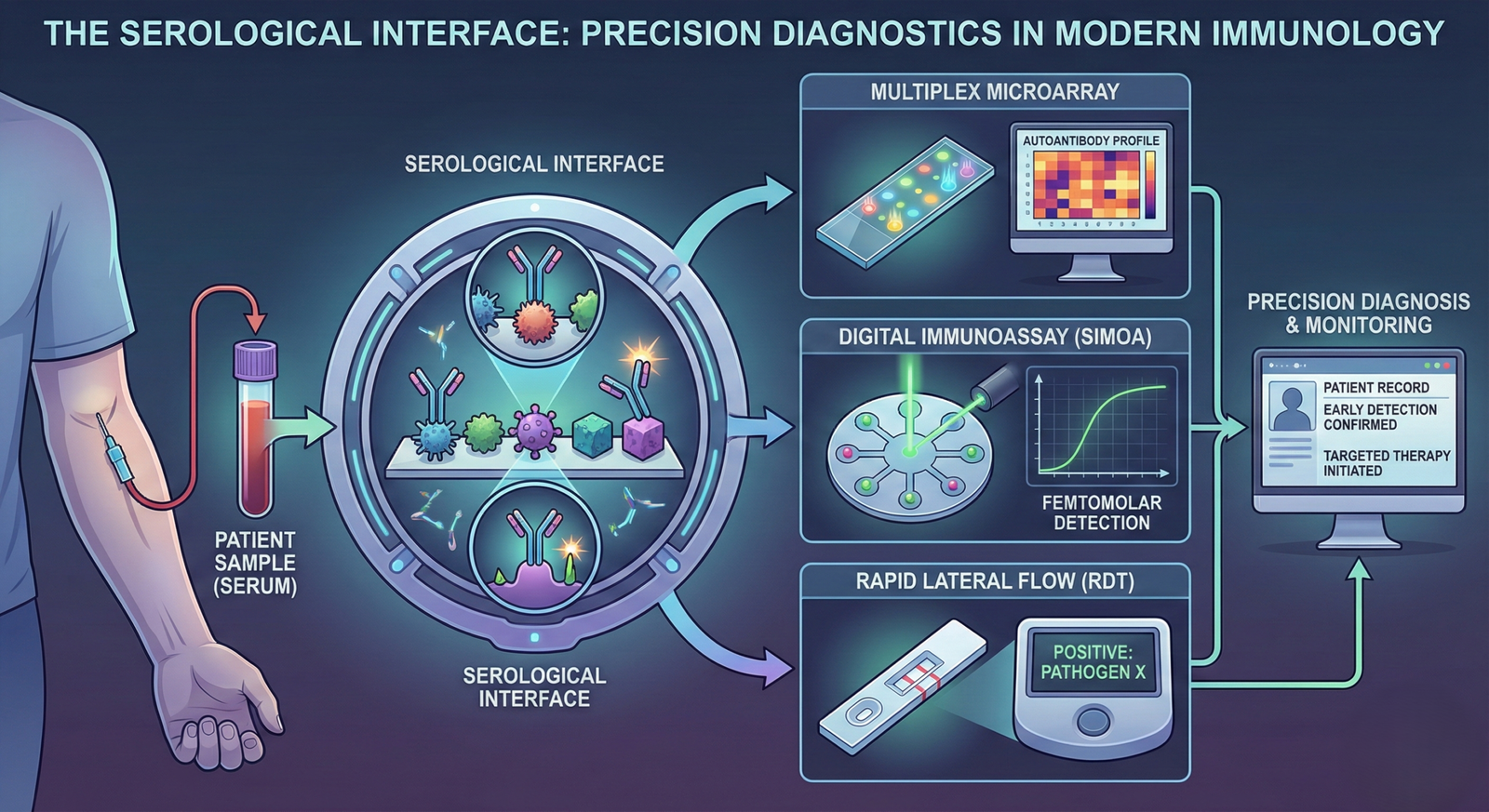
La prochaine génération d’immunologie diagnostique va bien au-delà de la simple découverte de nouveaux anticorps ; il s’agit de révolutionner notre façon de les détecter. Nous passons de la sérologie analogique (intensité de la couleur) à l’immunologie numérique (comptage moléculaire), et des analyses statiques à la surveillance continue.
L’inconvénient d’un test ELISA classique réside dans son bruit de fond. À des concentrations extrêmement faibles, il devient impossible de distinguer un signal faible des interférences dues au plastique.
Actuellement, un médecin suspectant une maladie auto-immune prescrit des tests séquentiels (d’abord les anticorps antinucléaires, puis les anti-ADN double brin, etc.). Cette procédure est longue. En revanche, l’avenir réside dans les puces à protéines .
Plus précisément, la puce : une lame de verre imprimée avec des milliers d’antigènes différents.
Par conséquent, le résultat : une carte thermique illustrant le répertoire d’anticorps du patient, son « immunonome » .
De plus, analyse des données : nous pouvons suivre la « propagation des épitopes » , un processus par lequel le système immunitaire étend son attaque d’une cible à une autre (par exemple, dans le lupus).
L’obligation de disposer de laboratoires centraux constitue un obstacle majeur. La technologie microfluidique (« laboratoire sur puce ») permet de résoudre ce problème.
Le domaine évolue de la détection de cibles uniques vers des puces multiplexes capables de tester simultanément 100 allergènes ou 50 auto-anticorps. Cependant, malgré cette révolution technologique, les règles fondamentales demeurent : la fiabilité repose sur la compréhension de la cinétique de liaison , de la « période fenêtre » et du risque de bruit biologique.